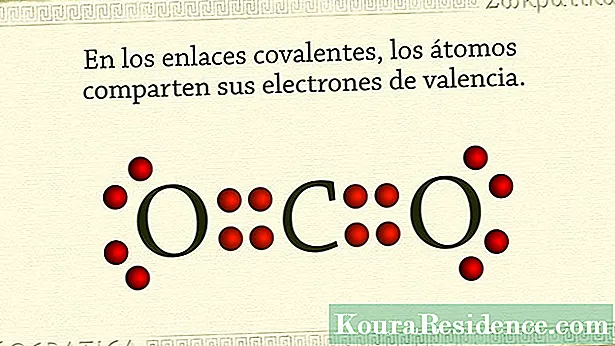
ទាំងពីរ សមាសធាតុគីមី ដោយសារធាតុគីមីត្រូវបានបង្កើតឡើងដោយម៉ូលេគុលហើយធាតុទាំងនេះត្រូវបានបង្កើតឡើងដោយអាតូម។ អាតូមនៅតែរួបរួមគ្នាដោយសារការបង្កើតអ្វីដែលគេហៅថា តំណភ្ជាប់គីមី.
នេះ ចំណងគីមីគឺមិនដូចគ្នាទាំងអស់៖ ជាទូទៅពួកគេពឹងផ្អែកលើលក្ខណៈអេឡិចត្រូនិកនៃអាតូមដែលពាក់ព័ន្ធ។ តំណភ្ជាប់មានពីរប្រភេទទូទៅបំផុត៖ មូលបត្របំណុលអ៊ីយ៉ុង និង មូលបត្របំណុល covalent ។
ជាធម្មតាចំណង covalent គឺជារបស់ទាំងនោះ កាន់អាតូមដែលមិនមែនជាលោហធាតុជាមួយគ្នា។ វាកើតឡើងដែលអាតូមនៃធាតុទាំងនេះមានអេឡិចត្រុងជាច្រើននៅក្នុងសែលខាងក្រៅរបស់វាហើយមាននិន្នាការរក្សាឬទទួលបានអេឡិចត្រុងជំនួសឱ្យការបោះបង់ចោល។
នោះហើយជាមូលហេតុដែលវិធីដែលសារធាតុទាំងនេះឬសមាសធាតុគីមីអាយកូសសម្រេចបាននូវស្ថេរភាពគឺតាមរយៈការចែករំលែកអេឡិចត្រុងមួយគូមិនមែនមកពីអាតូមនីមួយៗទេ តាមរបៀបនេះអេឡិចត្រុងមួយគូដែលបានចែករំលែកគឺជារឿងធម្មតាចំពោះអាតូមទាំងពីរហើយក្នុងពេលតែមួយរក្សាវាជាមួយគ្នា។ ក្នុង ឧស្ម័ន ឧទាហរណ៍អភិជនទាំងនេះកើតឡើង។ ផងដែរនៅក្នុងធាតុ halogen ។
នៅពេលដែលចំណង covalent កើតឡើងរវាងធាតុអេឡិចត្រូនិចដែលមានលក្ខណៈស្រដៀងគ្នាដូចជារវាងអ៊ីដ្រូសែននិងកាបូនចំណងត្រូវបានបង្កើតឡើង កូវ៉ាឡែនអាប៉ូឡា។ ឧទាហរណ៍នេះកើតឡើងនៅក្នុងអ៊ីដ្រូកាបូន។
ដូចគ្នាដែរម៉ូលេគុល homonuclear (បង្កើតដោយអាតូមដូចគ្នា) តែងតែបង្កើត មូលបត្របំណុលអាប៉ូឡា។ ប៉ុន្តែប្រសិនបើចំណងកើតឡើងរវាងធាតុនៃអេឡិចត្រូលីតខុសៗគ្នាដង់ស៊ីតេអេឡិចត្រុងខ្ពស់ត្រូវបានផលិតនៅក្នុងអាតូមមួយជាជាងអាតូមមួយទៀតដែលជាលទ្ធផលបង្គោលមួយត្រូវបានបង្កើតឡើង។
លទ្ធភាពទីបីគឺអាតូមពីរមានអេឡិចត្រុងមួយគូប៉ុន្តែអេឡិចត្រុងដែលបានចែករំលែកទាំងនេះត្រូវបានរួមចំណែកដោយអាតូមតែមួយប៉ុណ្ណោះ។ ក្នុងករណីនោះយើងនិយាយអំពី dative ឬសំរបសំរួលចំណង covalent.
សម្រាប់ក តំណភ្ជាប់ អ្នកត្រូវការធាតុមួយដែលមានគូអេឡិចត្រុងសេរី (ដូចជាអាសូត) និងធាតុមួយទៀតដែលខ្វះអេឡិចត្រុង (ដូចជាអ៊ីដ្រូសែន) ។ វាក៏ចាំបាច់ផងដែរដែលអេឡិចត្រូនិចមួយគូមានអេឡិចត្រូនិកគ្រប់គ្រាន់ដើម្បីមិនបាត់បង់អេឡិចត្រុងដើម្បីចែករំលែក។ ស្ថានភាពនេះកើតឡើងឧទាហរណ៍នៅក្នុងអាម៉ូញាក់ (NH4+).
នេះ សារធាតុ ដែលមានសមាសធាតុ covalent អាចកើតឡើងនៅក្នុងស្ថានភាពណាមួយ (រឹងរាវឬឧស្ម័ន) និងជាទូទៅ ពួកគេគឺជាមេកំដៅនិងអគ្គិសនីមិនល្អ.
ពួកគេជារឿយៗបង្ហាញ ចំណុចរលាយនិងពុះទាប និង ជាធម្មតារលាយក្នុងសារធាតុរំលាយប៉ូលដូចជាបេនហ្សេនឬកាបូនតេត្រាក្លរីតប៉ុន្តែមានភាពរលាយតិចតួចនៅក្នុងទឹក។ ពួកគេមានស្ថេរភាពខ្លាំង។
ឧទាហរណ៍ជាច្រើននៃសមាសធាតុឬសារធាតុដែលមានចំណង covalent អាចត្រូវបានផ្តល់ឱ្យ៖
- ហ្វ្លុយអូរីន
- ប្រូម៉ូន
- អ៊ីយ៉ូត
- ក្លរីន
- អុកស៊ីសែន
- ទឹក
- កាបូនឌីអុកស៊ីត
- អាម៉ូញាក់
- មេតាន
- ប្រូប៉ាអ៊ីន
- ស៊ីលីកា
- ពេជ្រ
- ក្រាហ្វិច
- រ៉ែថ្មខៀវ
- គ្លុយកូស
- ប៉ារ៉ាហ្វីន
- ម៉ាស៊ូត
- អាសូត
- អេលីយ៉ូម
- ហ្វ្រីន


